1. 概念・定義・病因・病態・予後
家族性高コレステロール血症(familial hypercholesterolemia:FH)は、高LDL-C血症、腱黄色腫、早期性冠動脈疾患を主な特徴とする遺伝的疾患です。主に常染色体優性遺伝形式をとり、LDL受容体、アポリポ蛋白B100(アポB-100)、Proprotein Convertase Subtilisin/Kexin type 9(PCSK9)が原因遺伝子とされています。これらはいずれもLDLの代謝に関わる蛋白であり、FH患者ではLDLが肝臓に取り込まれないため出生時より高LDL-C血症をきたします。FHホモ接合体では、血清総コレステロール(T-Cho)値は600~1200mg/dLと著明に上昇し、アキレス腱をはじめとする腱黄色腫が特徴的であり、最も重症な症例(FHホモ接合体)では、幼児期にすでに冠動脈狭窄や完全閉塞、大動脈弁狭窄や弁上狭窄を有する例が存在し予後は極めて不良です。このためFHホモ接合体は、国の特定疾患治療研究事業対象疾患(http://www.nanbyou.or.jp/entry/65)に指定されています。またFHヘテロ接合体では、血清T-Cho値は320~350mg/dLですが、個々の症例によるばらつきは大きく、血清T-Cho値高値の重症例ではホモ接合体同様に若年性冠動脈疾患を発症しやすく予後不良です。
2. 疫学
これまでの研究で、わが国におけるFH患者総数は、30万人以上と推定されており、FHホモ接合体患者は 100万人に1人以上の頻度で認められています。なお、FHヘテロ接合体患者は500人に1人以上の頻度と推定されてきましたが、最近の北陸地方における研究では、遺伝子診断によりFHホモ接合体は17万人に1人、FHヘテロ接合体は約200人に1人と推定している報告もあります。遺伝性脂質代謝疾患の中で、FHは最も高頻度にみられる疾患です。
3.診断基準
成人(15歳以上)FHヘテロ接合体の診断基準
FHヘテロ接合体はLDL-C値、腱黄色腫・皮膚結節性黄色腫及び家族歴から診断できる。
- 高LDL-C血症(未治療時のLDL-C180,g/dl以上)
- 腱黄色腫(手背、肘、膝などの腱黄色腫あるいはアキレス腱肥厚)あるいは皮膚結節性黄色腫
- FHあるいは 早発性冠動脈疾患の家族歴(2親等いないの血族)
- 続発性高脂血症を除外した上で診断する。
- 2項目以上が当てはまる場合、FHと診断する。FH疑いの際には遺伝子検査による診断を行うことが望ましい。
- 皮膚結節性黄色腫に眼瞼黄色腫は含まない。
- アキレス腱肥厚は軟線撮影により9mm以上にて診断する。
- LDL-Cが250mg/dL以上の場合、FHを強く疑う。
- すでに薬物治療中の場合、治療のきっかけとなった脂質値を参考とする。
- 早発性冠動脈疾患は男性55歳未満、女性65歳未満と定義する。
- FHと診断した場合、家族についても調べることが望ましい。
4. 標準治療
FHの治療の基本は、冠動脈疾患など若年齢で起きる動脈硬化症の発症及び進展の予防であり、早期診断とLDL-C値を可能な限り低下させる治療が最も重要です。出来るだけ早期に診断を下し、以下のような治療を行います。
- 生活習慣の是正
魚介類や野菜を中心とした食生活を行うと同時に、運動療法や禁煙も非常に重要です。コレステロール摂取基準は一般には撤廃されましたが、本疾患患者ではコレステロールを多く含む食品の摂取の制限は大切です。ただし生活習慣の改善のみでは、LDL-C値を治療目標値まで低下させることは困難なことがほとんどです。 - 内服治療
薬物療法として、スタチン、エゼチミブ、プロブコール、レジンなどのLDL-C低下薬の内服を行います。これらの治療により、治療目標値であるLDL-C 100mg/dL以下(ないし未治療時のLDL-Cの半分値)を目指します。しかし重症FHヘテロ接合体やFHホモ接合体では、治療目標値まで到達しない症例も存在します。FHホモ接合体に対しては、2016年からMTTP阻害剤が上市されました。一定程度のLDL-C低下効果が期待できますが、副作用として脂肪肝、肝障害、脂肪性下痢などがあり、FHヘテロ接合体では適応がありません。 - PCSK9阻害薬
本邦でも2016年に、生活習慣病領域で初の抗体医薬である、ヒト抗PCSK9モノクローナル抗体が上市され、保険診療が可能になりました。FHヘテロ接合体で、スタチンを最大容量投与してもLDL-C値が治療目標値に到達しない症例に対し、2週間に一度の割合で皮下注射により投与します。FHヘテロ接合体では、スタチンやエゼチミブなどの内服療法のみではコントロールが十分ではなかった重症例に対しても効果が期待でき、当科でも数多くの症例でLDL-C管理目標値が達成できるようになっています。 - LDLアフェレーシス
FHホモ接合体や一部の重症FHヘテロ接合体では薬物療法の効果が乏しく、その場合には1~2週に1回のLDLアフェレーシス(吸着法)によってLDLを取り除くこと治療を行います。導入開始の時期が遅くなるほど動脈硬化症が進行してしまい予後が悪くなるため、できる限り早期に治療を開始することが勧められます。
5. 大阪大学で開発中の新しい治療法:重症家族性高コレステロール血症に対する同種幹細胞移植療法について
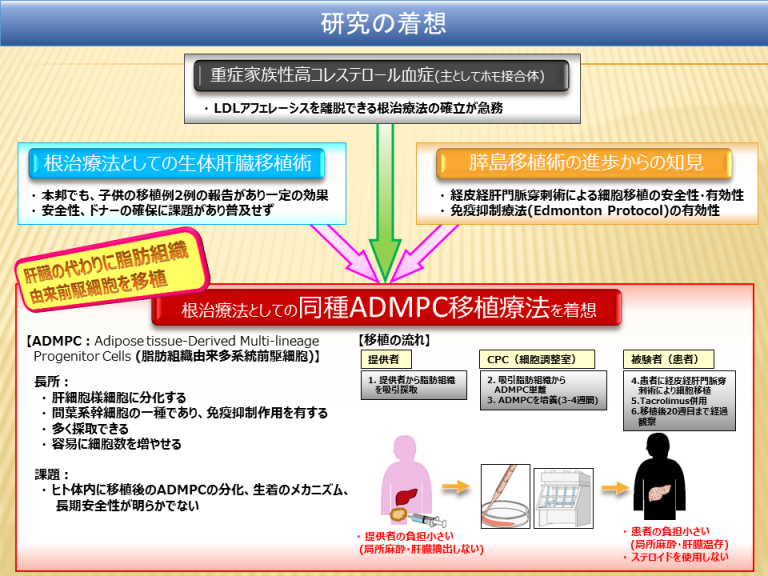
主としてホモ接合体の、重症家族性高コレステロール血症患者においては、薬物治療のみでは十分なLDL受容体の機能を回復できず、LDLアフェレーシス等の治療が必要となりますが、患者さんのQOL低下を伴い大きな負担となります。一方で、何らかの方法で肝臓のLDL受容体を回復する、“根治的な”治療法を確立できれば、LDLアフェレーシス等から離脱できる可能性があります。一つの方法は、LDL受容体を有している提供者からの肝臓移植であり、本邦でも2例の報告があるものの、移植手術の安全性、ドナーの確保などの課題があり普及しているとは言えません。
一方で、近年、一型糖尿病においては、細胞治療の技術が進歩し、臓器ではなく膵島という細胞単位での移植の技術が確立しつつあります。そこで、我々は、これらを組み合わせて、提供者から肝臓の代わりに脂肪組織を局所麻酔下に吸引採取し、LDL受容体を有した脂肪組織由来の幹細胞を採取し、細胞培養で幹細胞数を増やし、経皮経肝的にカテーテルから細胞を患者に移植するという治療(同種脂肪組織由来多系統前駆細胞移植療法)の開発を世界に先駆けて行い、現在日本医療研究開発機構(AMED)再生医療実用化研究事業として臨床研究を行っています。

詳細はこちら。
6. 治療に関するお問い合わせ
大阪大学医学部附属病院循環器内科では、これまでFHに対して精力的に診療、研究を続けています。LDL-C異常高値症例はもちろん、臨床的FHと診断される症例については、いつでもお気軽にご相談下さい。
特に患者様のLDL-C検査値が
- 未治療時 LDL-C>250mg/dL
- 第1世代スタチン使用時 LDL-C>200 mg/dL
- ストロングスタチン使用時 LDL-C>150 mg/dL
のような場合、FHが強く疑われます。当科ではFHについても診断の後、治療初期のの動機付けをきちんと行った上で、内服薬を調整し、場合により抗PCSK9抗体医薬の導入を行い、病病連携、病診連携にて治療を継続させていただきます。
ご紹介の患者様がいらっしゃる場合は、当院ネットワーク部を通じて、当科 虚血・脂質外来(小関、西田)をご予約ください。
当科外来表はこちら。
またLDLアフェレーシスを要する重症例では、同種脂肪組織由来多系統前駆細胞移植療法の臨床研究をご紹介しております。